- ★Google+
- ★Hatena::Bookmark
創価大学工学部生命情報工学科の佐々木紀彦研究員、西原祥子教授らによる論文「ラックダイナック糖鎖構造は、LIF/STATシグナルを制御して、マウスES細胞の自己再生に関わっている」が、米国幹細胞関連雑誌『Stem Cells』電子版に掲載された。
ES細胞がどのようにして維持されているかを解明することは、ES細胞やiPS細胞の再生医療や各種産業への応用において、大変重要である。マウスES細胞の自己再生には、LIF/STAT3シグナルが関わっていることはよく知られている。しかし、ヒトES細胞やヒトiPS細胞、またこれらのヒト幹細胞と類似した発生段階にあると考えられているマウスエピブラスト様幹細胞では、LIF/STAT3シグナルは幹細胞維持に働かない。現在まで、この違いについての分子機構および、なぜこの様なことが起こるかは、解明されていなかった。
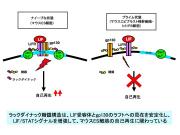
このたび、創価大学工学部生命情報工学科の佐々木紀彦研究員、西原祥子教授らは、細胞表面のラックダイナックという特殊な糖鎖構造がLIF/STAT3シグナルに関わっており、LIF受容体とそれと複合体を形成するgp130上にこの糖鎖がないと、これらがラフト/カベオラ(*)に局在できず、LIF/STAT3シグナルを強く誘起できないため、マウスES細胞のようなナイーブな状態に細胞を保つことができないことを明らかにした。
マウスES細胞では、ラックダイナック糖鎖構造とそれを合成する糖転移酵素は高発現している。この糖転移酵素をノックダウンして発現を抑えると、LIF受容体とgp130はラフト/カベオラに局在しなくなり、LIF/STAT3シグナルは弱まり、自己再生能を維持できなくなった。一方、発生段階が異なるマウスエピブラスト様幹細胞とヒトiPS細胞では、ラックダイナック糖鎖構造の発現は非常に低く、受容体とgp130はラフト/カベオラに局在していなかった。さらに、糖転移酵素をノックダウンすると、マウスエピブラスト様幹細胞をナイーブな本来のマウスES細胞に戻すことができなくなった。
これらの事実から、ナイーブな状態にあるマウスES細胞とプライム状態にあるヒトES細胞、ヒトiPS細胞、マウスエピブラスト様幹細胞のLIF感受性の違いは、LIF受容体とgp130上のラックダイナック糖鎖構造の発現の違いによるものであり、ラックダイナック糖鎖構造は、ナイーブな状態の誘導と維持に必要であることが明らかになった。
この研究をさらに発展させることにより、遺伝子導入や細胞の安定維持が難しいヒトES細胞やiPS細胞を、より扱いやすいナイーブな状態に容易に誘導することが可能になると期待される。
※この研究は、文部科学省 私立大学戦略的研究基盤形成支援事業 「モデル生物による in vivo 糖鎖生物学 - ES細胞から病態モデルへ」 (研究代表者:西原祥子教授)の一部支援で行われたもの。
*ラフト/カベオラ:
細胞膜には、特徴のある糖脂質が集合した脂質ラフト(マイクロドメイン)がある。その中で、カベオリンを含むものをカベオラと呼んでいる。これらのラフトには、さまざまなシグナル分子受容体やシグナル伝達分子であるsrcファミリーやGタンパク質が集合し、より効率的なシグナルの伝達を行うと考えられている。
▼本件に関する問い合わせ先
創価大学 広報部
〒192-8577 東京都八王子市丹木町1-236
TEL: 042-691-9442
FAX: 042-691-9300
大学・学校情報 |
|---|
| 大学・学校名 創価大学 |

|
| URL https://www.soka.ac.jp/ |
| 住所 東京都八王子市丹木町1-236 |
| 建学の精神に基づき、地域社会や地球社会の課題と真摯に向き合い、人々の幸福と世界の平和の実現に貢献する「創造的人間」、すなわち、価値創造を実践する「世界市民」の育成を目指します。 そのために、たしかな「知力」を基盤とし、不確かな未来を切り開く「創造性」を発揮する力、協働する人々の価値観や理念など「多様性」を受容(寛容)する力を育む教育に取り組みます。 |
| 学長(学校長) 鈴木 将史 |
 大学探しナビで創価大学の情報を見る
大学探しナビで創価大学の情報を見る