赤い光でピンポイントに「リン含有プロドラッグ」を放出する技術を開発〜金ナノクラスターを活用した、光によるがん治療へ向けた新たな一歩〜
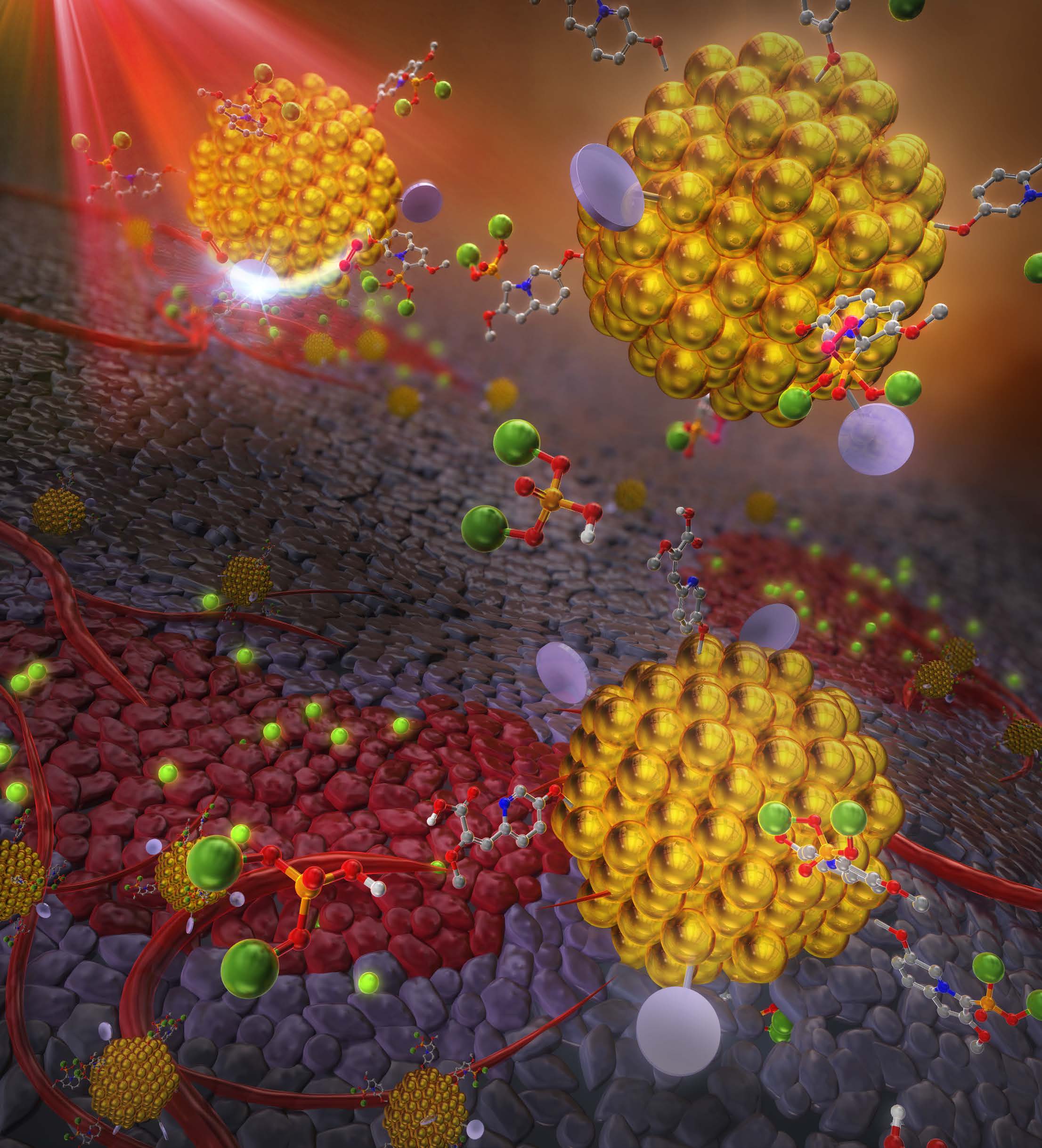
本研究成果は、副作用を抑えつつがん細胞を狙い撃ちにする新たな光化学療法や、薬剤耐性がんへの治療応用が期待されます。
本研究は、米国化学会誌『Journal of the American Chemical Society (JACS)』のオンライン版に掲載されました。
【背景】
光を用いて特定の場所・タイミングで薬を放出する技術は、副作用の少ない治療法として長年注目されています。特に、光線力学療法(PDT*3)は光増感剤と光を用いて活性酸素(一重項酸素*4)を発生させ、がんを治療する低侵襲な手法として臨床でも確立されています。しかし、一重項酸素は寿命が短く、拡散できる範囲が極めて狭いため、光が当たったごく一部の範囲の外にいるがん細胞が生き残り、再発につながるという課題がありました。
これを解決するため、光による一重項酸素の発生と「化学療法薬(抗がん剤)の局所的な放出」を組み合わせる戦略が模索されています。特に、細胞内で重要な働きをする「リン」を含んだ薬(例:抗がん剤のゲムシタビン*5のリン酸化体など)の放出技術が求められていました。ゲムシタビンは、細胞内でリン酸化されて初めて効果を発揮しますが、がん細胞はこのリン酸化酵素を減らすことで「薬剤耐性」を獲得してしまいます。あらかじめリン酸化された状態の薬を光で放出できれば、この耐性の原因となる過程をスキップ(バイパス)し、効果的にがん細胞を攻撃できると考えられます。
しかし、生体の深部まで届く「長波長の光(赤色〜近赤外光)」を使って、リン含有化合物を安定かつ効率的に放出できる実用的な分子の設計は、これまで極めて困難でした。
【研究手法と成果】
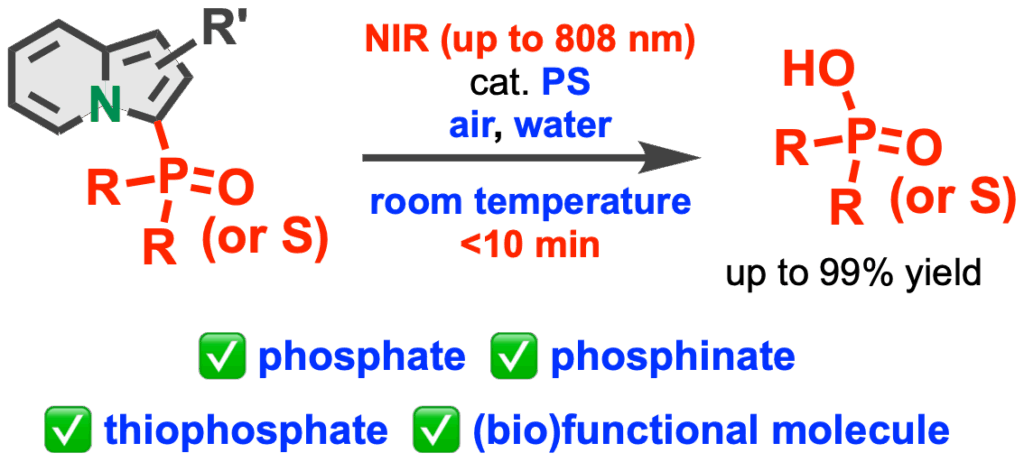
共同研究グループは、加水分解されにくい「炭素–リン結合(C(sp2)−P結合)」を持つ、インドリジンと呼ばれる骨格に着目しました。独自の合成手法により、ゲムシタビンを含む様々なリン化合物をインドリジン骨格に組み込んだ化合物を開発しました。
この化合物に触媒量の光増感剤を加え、生体に優しい660〜808 nmの赤色/近赤光を当てると、空気中の酸素と水が反応に関わり、炭素–リン結合が切断されて目的のリン化合物が高い収率で放出される(アンケージングされる)ことを見出しました。さらに、光増感剤が作り出した「一重項酸素」がこの結合切断の引き金となっているメカニズムを解明しました。
研究グループは、この反応を実際の生体環境(がん細胞)で機能させるため、直径わずか約1ナノメートルの「金ナノクラスター*6」を土台とした分子集合体を合成しました。この金ナノクラスターの表面には、以下の3つの機能を搭載しています。
・抗がん剤のプロドラッグ:インドリジンで保護(ケージ化)されたゲムシタビン
・がん細胞の標的化分子:がん細胞に集まりやすい環状RGDペプチド
・光増感剤:クロロフィル由来の赤色光を吸収する分子
この多機能な金ナノクラスターをヒト子宮頸がん由来のHeLa細胞に取り込ませた後、細胞外のクラスターを洗い流し、赤色光(660 nm)を2分間照射しました。その結果、光照射直後から経時的にがん細胞の細胞死(アポトーシス)が誘発され、48時間後にはほぼ完全に死滅することが確認されました。さらに、細胞周期解析により、光照射に伴って放出されたゲムシタビンがDNA合成を阻害し、遅延型の細胞毒性を発揮することが明らかとなっています。一方、光非照射下や正常な細胞に対しては、本クラスターの毒性が低く抑えられることも示されました。
【今後の期待】
今回開発した「一重項酸素を駆動力とした炭素–リン結合の切断」という新しいアプローチは、組織透過性の高い赤色・近赤外光を利用できる画期的な手法です。金ナノクラスターと組み合わせることで、がん細胞だけを狙い、光を当てた場所・タイミングでのみ強力な抗がん剤を活性化させることが可能になります。将来的には、従来の光線力学療法(PDT)の限界を突破し、薬剤耐性を持った深部のがんに対しても有効な、副作用の少ない新たな光化学療法や創薬候補化合物の開発に繋がることが期待されます。
【補足説明】
*1 プロドラッグ
体内(または標的部位)で代謝や特定の反応を受けることで、初めて薬としての効果を発揮するように設計された化合物のこと。
*2 アンケージング (Uncaging)
薬などの機能性分子を一時的に不活性な状態(ケージに入れた状態)にしておき、光などの外部刺激によってその保護基(ケージ)を外し、元の活性な状態に戻す(放出する)手法のこと。
*3 光線力学療法 (PDT: Photodynamic Therapy)
光増感剤を体内に投与し、がんに集まったところで特定の波長の光を照射し、発生した活性酸素(一重項酸素など)によってがん細胞を破壊する治療法。
*4 一重項酸素
通常の酸素分子より高いエネルギー状態にある活性酸素の一種。寿命が短く移動できる距離が非常に短いため、発生した周囲の細胞や分子にのみ強力な酸化作用を及ぼす。
*5 ゲムシタビン
膵臓がんや肺がんなどで広く使われている抗がん剤。細胞内に取り込まれた後、酵素によってリン酸化されることでDNAの合成を阻害し、効果を発揮する。
*6 金ナノクラスター
金原子が数十から数百個集まった、1〜2ナノメートル程度の極小の金粒子。生体適合性が高く、体内からの排出も容易なため医薬品のキャリアとして注目されている。
【共同研究グループ】 *職位・学年等は研究当時の情報
■同志社女子大学薬学部
渡邊 賢司(特別任用助教)、高田 生琉(医療薬学科4年次生)、野村 夏未(医療薬学科4年次生)、笹田 莉生(医療薬学科3年次生)、戴 鈺綺(医療薬学科3年次生)、知名 秀泰(特別任用助教)、根木 滋(教授)、山本 康友(教授)
■同志社大学理工学部
山本 莉子(大学院生)、小橋 寛人(大学院生)、牧 孝多朗(大学院生)、北岸 宏亮(教授)、小寺 政人(教授)
■九州大学大学院薬学研究院/東京科学大学総合研究院生体材料工学研究所
丹羽 節(教授)
東京科学大学総合研究院生体材料工学研究所
細谷 孝充(教授)
【研究支援】
本研究は、日本学術振興会(JSPS)科学研究費助成事業(基盤研究(C)JP22K05325)および、同志社女子大学の個人研究助成(2025-12)による支援を受けて行われました。
【原著論文情報】
タイトル: Singlet-Oxygen-Driven C(sp2)–P Bond Cleavage Enables Red-Light Uncaging of Phosphorus(V) Prodrugs on Gold Nanoclusters
著者: Kenji Watanabe, Ikuru Takada, Riko Yamamoto, Hiroto Kobashi, Kotaro Maki, Natsumi Nomura, Rio Sasada, Iuchi Tai, Hideyasu China, Takashi Niwa, Takamitsu Hosoya, Hiroaki Kitagishi, Shigeru Negi, Masahito Kodera, and Yasutomo Yamamoto
雑誌名: Journal of the American Chemical Society
https://doi.org/10.1021/jacs.6c00254
本件に関するお問い合わせ先
同志社女子大学薬学部医療薬学科 創薬有機化学研究室
特任助教 渡邊 賢司
TEL:0774-65-8652 E-mail:k-watanabe@dwc.doshisha.ac.jp
メディア関連の⽅へ
取材をご希望の⽅は、お⼿数ですが下記問い合わせ先までご連絡をお願いいたします。
同志社女子大学広報課長 川添 麻衣子
TEL:0774-65-8631 FAX:0774-65-8632
E-mail:koho-t@dwc.doshisha.ac.jp
本件に関するお問い合わせ先
同志社女子大学
広報課長 川添麻衣子
- 住所
- 京都府京田辺市興戸南鉾97-1
- TEL
- 0774658631
- koho-t@dwc.doshisha.ac.jp