インフルエンザウイルス感染防御に有効な免疫システムを解明 新たなインフルエンザワクチンの開発に大きな期待
本件に関する論文2本が、令和元年(2019年)9月26日(木)22:00(日本時間)、免疫学分野のトップジャーナルである”Journal of Experimental Medicine”に同時にオンライン掲載されました。
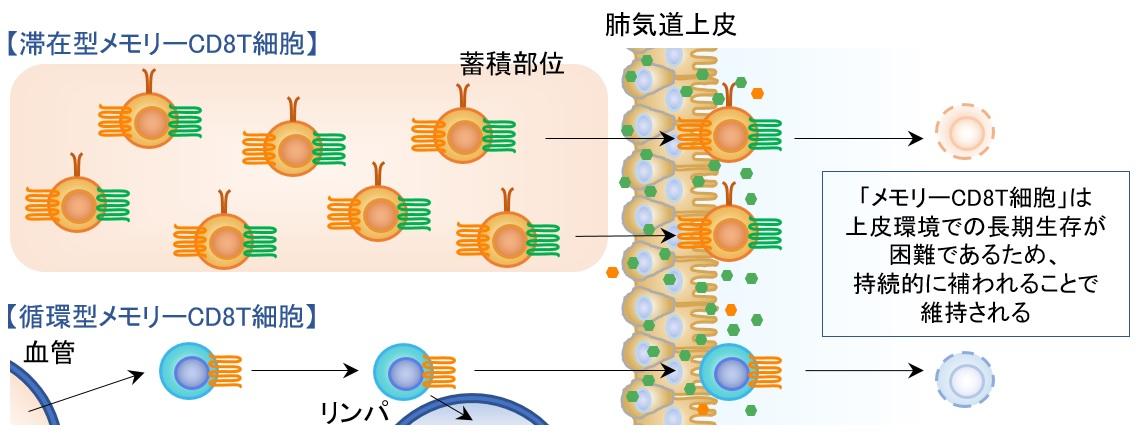
●滞在型メモリーCD8T細胞が、インフルエンザウイルス感染防御のため肺気道上皮に持続的に供給されていることを発見し、その仕組みを解明
●感染細胞を直接破壊するCD8T細胞を誘導・維持することができれば有効な感染対策となる
●あらゆるインフルエンザウイルス株に有効な新しいワクチンの開発に大きな期待
2. 研究の背景と先行研究
現在のインフルエンザワクチンは、変異しやすいウイルス表面タンパク質を標的とするため、特定の型のウイルスにしか効果を示しません。また、ウイルス侵入門戸である呼吸器粘膜における免疫応答誘導効果が期待できないため、感染そのものを阻止することは不可能です。一方、インフルエンザウイルス感染防御を担うCD8T細胞(※2)は、あらゆるウイルス株に共通するウイルス内部タンパク質を標的として感染細胞を直接破壊するため、その維持機構を解明し、呼吸器粘膜に効果的に誘導・維持することができれば、インフルエンザウイルス感染防御の有効な手段になると考えられます。
メモリーCD8T細胞には「循環型」(※3)と「滞在型」があり、滞在型メモリーCD8T細胞はウイルスを排除した後も組織内に長期間滞在し、再感染に対する防御の最前線を担うことが知られています。高村らの研究グループは、平成28年(2016年)に発表した先行研究で、肺における滞在型メモリーCD8T細胞の蓄積部位を特定しており、さらに詳細な維持機構を解明することが期待されていました。
3. 今回の研究内容
今回の研究成果は、近畿大学医学部、近畿大学薬学部、近畿大学アンチエイジングセンター、大阪大学、東京理科大学、理化学研究所、大阪大谷大学、米国エモリー大学、カリフォルニア大学、ペンシルベニア大学との共同研究によるもので、肺気道上皮の滞在型メモリーCD8T細胞が、循環型とは完全に独立して長期維持されていることを立証し、さらにその持続的供給機構を解明しました。
高村らの研究グループは、ウイルスが最初に感染する肺気道上皮細胞間に存在する肺気道メモリーCD8T細胞に関して研究を進め、1)肺気道環境はメモリーCD8T細胞の長期生存に適さないため、継続的に新しい細胞を補わないと防御に有効な細胞数を維持できないこと、2)肺気道にメモリーCD8T細胞を持続供給しているのは循環系ではなく、高村らが先行研究で示した肺実質内に存在するメモリーCD8T細胞の蓄積部位であること、3)この細胞移行には、肺実質メモリーCD8T細胞(※4)に特徴的に発現する受容体が関わっていることを発見しました。
4. 今後の展開
高村らの研究によって、肺気道上皮にメモリーCD8T細胞を持続供給する仕組みが解明されましたが、既存の全身免疫型ワクチンでは肺気道メモリーCD8T細胞を誘導することが困難であることも示されました。今後さらにその維持機構の詳細を明らかにし、CD8T細胞を感染局所に効果的に誘導・維持することができれば、あらゆるインフルエンザウイルス株に有効な新しいワクチンの開発が可能になります。
・掲載誌:
ロックフェラー大学出版局が発行する免疫学分野のトップジャーナル
【論文1】
・論文名:
・著 者:
近畿大学医学部…加藤茂樹、升本知子、勝島朝美、宮澤正顯
大阪大学微生物病研究所…本園千尋
東京理科大学生命医科学研究所…島岡猛士、上羽悟史、松島綱治
近畿大学薬学部…松尾一彦、中山隆志
理化学研究所・生命医科学研究センター…宮内浩典、久保允人
大阪大谷大学薬学部…戸村道夫
【論文2】
・論文名:
・著 者:
近畿大学医学部…升本知子
エモリー大学医学部微生物・免疫学教室…Paul R. Dunbar, Emily K. Cartwright, Sarah L. Hayward, Daniel T. McManus、Jacob E. Kohlmeier(責任著者)
東京理科大学生命医科学研究所…島岡猛士、上羽悟史、松島綱治
カリフォルニア大学医学部…津久井達哉
ペンシルベニア大学医学大学院微生物学教室・免疫学センター…倉知慎
6. 研究詳細
メモリーT細胞はその循環形態により、リンパ節及び血流を循環するセントラルメモリー(central memory T cell: TCM)、末梢組織と血流間を循環するエフェクターメモリー(effector memory T cell: TEM)、循環することなく末梢組織に滞在し続ける滞在型メモリー(tissue-resident memory T cell: TRM)に分類されます。末梢組織に存在するメモリーCD8T細胞の大部分はTRMで、再感染時の防御免疫に重要な役割を果たしています。高村らの研究グループは、ウイルス感染マウス同士を外科的に結合し、2匹のマウスの血流を共有させるパラビオーシス法を用い、循環型(TCMおよびTEM)と滞在型(TRM)とを効果的に識別することで、インフルエンザウイルス感染マウス肺におけるCD8TRM蓄積部位を特定しました。即ち、肺CD8TRMは感染によって生じた肺組織の障害を修復するために形成された細胞集塊に局在していることを突き止め、この部位を「修復関連メモリー貯蔵部位」(Repair-associated memory depot: RAMD)と命名しました(Takamura et al. Journal of Experimental Medicine, 2016;213:3057-3073)。同研究グループは更なる研究を進め、全身を循環するTCMおよびTEMを除去しても肺上皮細胞間に存在する肺気道CD8TRM、および肺実質(RAMD)のCD8TRMは維持されることを発見しました。また、これら細胞集団のT細胞受容体レパートリー(※5)の大部分が一致することより、修復関連メモリー貯蔵部位のCD8TRMが肺気道CD8TRMを補っている源であることが示されました。循環型メモリーCD8T細胞とは異なり、修復関連メモリー貯蔵部位のCD8TRMは活性化型の表現系を示し、活性化に伴いケモカイン受容体CXCR6(※6)を発現することも解りました。一方、肺上皮細胞では定常時においてもCXCR6のリガンド(※7)であるCXCL16が常に発現しており、これがCXCR6を発現するRAMDのCD8TRMの上皮間への持続的移行を可能としていることも判明しました。
7. 用語解説
(※1)滞在型メモリーCD8T細胞…感染部位などの末梢組織に滞在し続け、再感染時に即座に感染細胞を認識・破壊するメモリーCD8T細胞
(※2)CD8T細胞…ウイルス感染細胞を認識・破壊するTリンパ球
(※3)循環型メモリーCD8T細胞…全身のリンパ、血液間(一部末梢組織を含む)を循環しているメモリーCD8T細胞
(※4)肺実質メモリーCD8T細胞…ウイルス感染後の肺実質の修復巣に蓄積しているメモリーCD8T細胞
(※5)T細胞受容体レパートリー…T細胞受容体構成成分の種類
(※6)ケモカイン受容体CXCR6…細胞の移行を調節する分子のうち、ケモカインCXCL16に反応する受容体
(※7)リガンド…受容体に結合し、反応を引き起こす物質
本件に関するお問い合わせ先
- 住所
- 〒577-8502 大阪府東大阪市小若江3-4-1
- TEL
- 06‐4307‐3007
- FAX
- 06‐6727‐5288
- koho@kindai.ac.jp