慢性腎臓病を治る病気に〜 進行した腎線維化の回復に成功、慢性腎臓病の新規治療薬の開発に希望 〜
慢性腎臓病(CKD)は腎組織の線維化により進行する疾患で、効果的な治療手段の確立が重要な医療ニーズとなっています。
私たちは、線維化を引き起こす新たな分子経路「PKM2*1) -CCN2*2) シグナル経路」を特定し、PKM2阻害剤である化合物3k*3) がマウス慢性腎臓病モデルの腎線維化と尿細管萎縮を改善することを発見しました。
• 化合物3kの経口投与により、マウスCKDモデルにおける腎萎縮と線維化が顕著に抑制されました。
• 傷害1日後から投与を開始した早期治療群だけでなく、腎線維化が進行してから投与を開始した遅延治療群でも有効性が確認されました。つまり、進行した慢性腎臓病の症状を経口薬で回復することに成功しました。
• 症状が回復した腎臓では、線維化の促進因子であるCCN2の発現が抑制されていました。培養ヒト腎細胞の障害モデル系を用いた解析により、3k投与下ではPKM2の核移行が抑制され、さらに線維化関連遺伝子の転写調節因子であるYAP1*4) 、β-カテニン*5) の核移行も減少する結果、遺伝子発現レベルで線維化が抑制されることが示されました。
• PKM2が転写補助因子としてYAP1およびβ-カテニンと複合体を形成し、CCN2発現を誘導する、新たな線維化シグナル経路が明らかとなりました。
• 本研究により、PKM2を阻害して腎機能を回復する、画期的なCKD新規治療薬開発への道筋が拓かれました(特許出願中)。
• 新たな治療薬を医療現場に一日も早く届けるべく、熱意のある共同研究者を募集しています。
■概要■
慢性腎臓病(CKD)の国内患者数は約2,000万人です。腎臓が硬くなる「線維化」が進行すると治療方法はなく、低下した腎機能の回復はほぼ不可能であるとされています。
埼玉医科大学(学長 竹内 勤)の岡田 浩一 教授(医学部・腎臓内科)、小坂井 和歌子 助教(医学部・腎臓内科、研究統括センター)、佐藤 哲也 准教授(医学部・中央研究施設)、井上 勉 教授(医学部・腎臓内科)らの研究グループは、マウスCKDモデルを用いて、ピルビン酸キナーゼM2(PKM2)阻害剤である化合物3kが、進行した腎臓の線維化を回復できることを世界で初めて発見しました。これは、回復不可能とされていた慢性腎臓病に対する新規治療薬の開発戦略を示す重要な発見です。経口薬による治療が可能になれば、透析導入の回避により、患者の生活の質の維持・向上と、年間1.5兆円と試算される透析医療費の抑制に貢献することが期待されます。本成果は2025年12月号のJournal of Biological Chemistry誌にオンライン掲載されました。
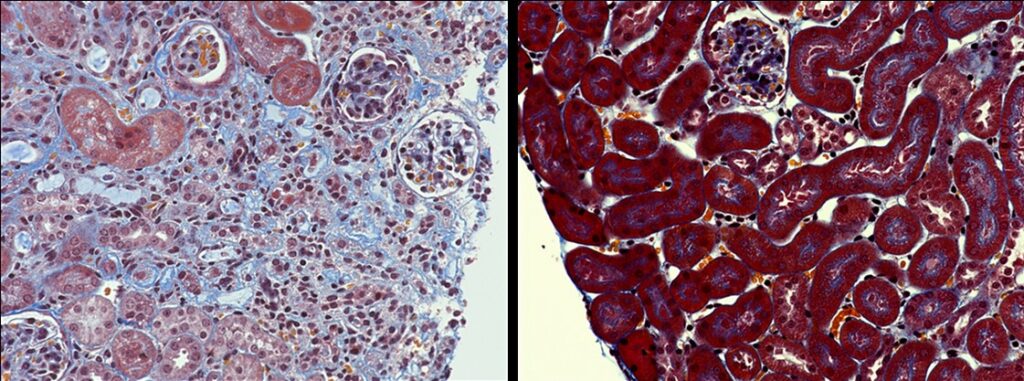
虚血再還流による腎障害の誘導後14日で、線維化が進行し腎臓の構造が損なわれる(左図:ミズイロの領域)。この期間に化合物3kを投与すると、線維化が抑制され正常構造が保たれる(右図:アカ-褐色の領域)。(マッソン・トリクローム染色、顕微鏡写真)
■研究背景■
腎臓の機能が低下すると体内の老廃物を排出できなくなり、最終的には透析や腎移植が必要になります。現在、RAA系阻害薬*6) やSGLT2阻害薬*7) など腎臓を保護する薬はありますが、いずれも病気の進行を遅らせる効果にとどまり、低下した腎機能は回復できませんでした。
慢性腎臓病(CKD)では持続的な腎機能の低下が認められますが、その進行に関わるのが腎臓の線維化という現象です。線維化が誘導されると、正常な組織がコラーゲンなどの硬い線維に置き換わり、腎臓は硬く縮んでしまいます。この線維化は糖尿病、高血圧、腎炎などさまざまな原因から腎臓にストレスがかかることで起こります。傷害を受けた腎臓では低酸素や虚血が進行するため、細胞のエネルギー産生様式が変化しますが、この代謝の変化が線維化を促進することが分かってきました。
本研究で注目したPKM2は、この代謝異常の鍵を握る酵素です。PKM2は通常は細胞質で代謝に関わっていますが、腎臓が傷つくと核内に移動し、線維化を引き起こす遺伝子のスイッチを入れる転写補助因子として働きます。研究グループは、PKM2を阻害すれば線維化を止められるのではないかと考え、本研究に着手しました。
■研究内容■
まず、マウス慢性腎臓病モデル(UIRIモデル)を用いて、PKM2阻害剤である化合物3kの効果を検討しました(図2)
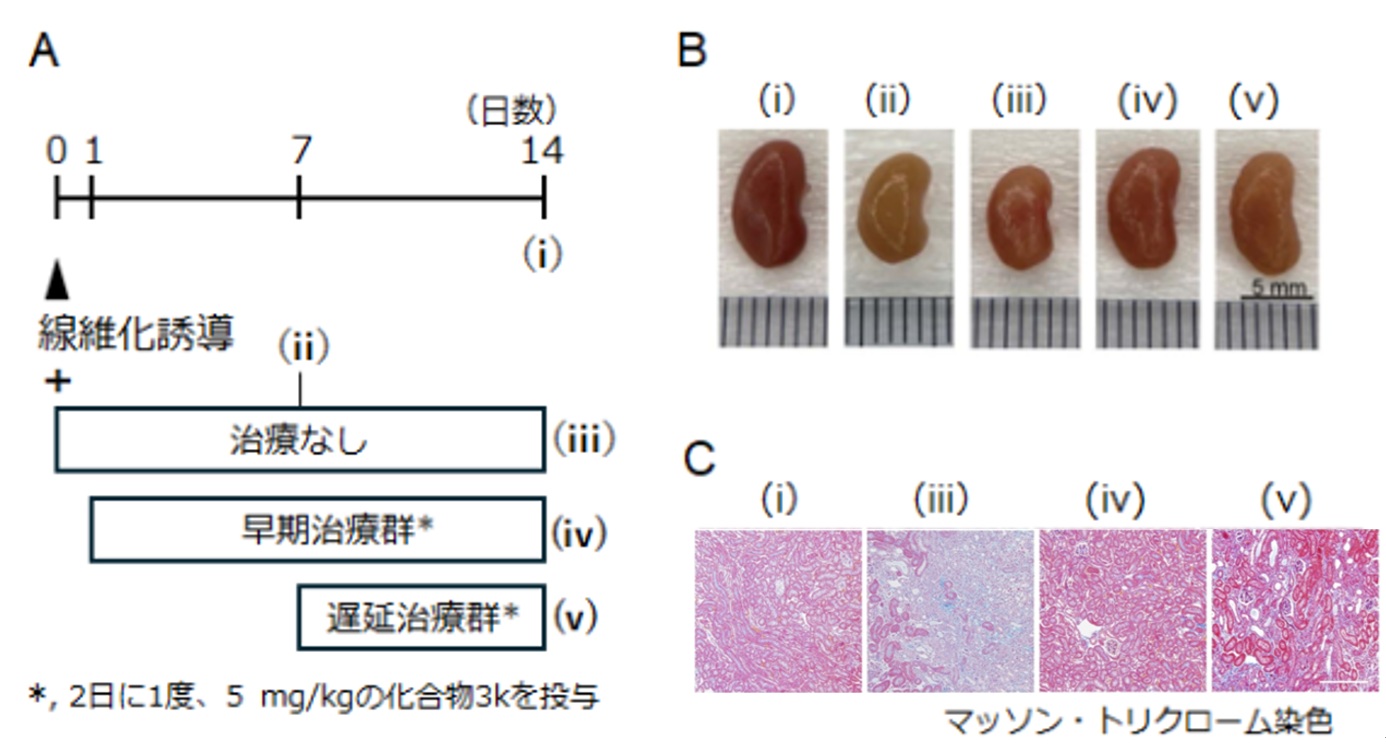
A, 実験のプロトコル。正常コントロール(i; 誘導処理なし)、線維化誘導処置後、治療なしでの経過(ii-7日後、iii-14日後)と治療群(iv-1日後、v-7日後より14日後まで化合物3kを投与した)を解析した。B, 7日後(ii)および14日後(iii)に観察される腎臓の萎縮が3k投与により抑制された(ivおよびv)。C, 線維化の進行(iii, ミズイロの領域)に対し、化合物3kは抑制または回復(ivおよびv)効果を示した。(Kosakai et al. (2026) JBC, doi:10.1016/j.jbc.2025.111029より改変)
UIRIモデルは虚血-再灌流による腎傷害で腎臓の線維化を誘導する実験系です(図2A)。進行性の腎萎縮と線維化が観察されますが、化合物3kの投与により、腎萎縮(図2B)と線維化(図2C)が顕著に抑制されました。注目すべきことは、傷害1日後から投与を開始した早期治療群だけでなく、7日後から投与を開始した遅延治療群でも、有効性が確認されたという点です(図2. ivおよびv)。
線維化を呈した腎臓では、CCN2など線維化促進タンパク質の遺伝子発現量が上昇していますが、この現象を3k投与が抑制していることが分かりました。蛍光免疫染色で、細胞増殖や線維化関連遺伝子の発現促進因子YAP1の発現・局在を検討すると、線維化が進んだ組織ではより強い染色像が得られ、管状構造をとる細胞の細胞質および核内での局在が顕著となっていました(図3. 治療なし)。また、LTL染色(近位尿細管のマーカー)により、尿細管の損傷と萎縮が起きていることが確認されました。早期治療群と遅延治療群ではともに、これらの変化が認められず(図3. 早期および遅延治療群)、化合物3kによって線維化を促進する遺伝子発現が抑制されるということが示されました。
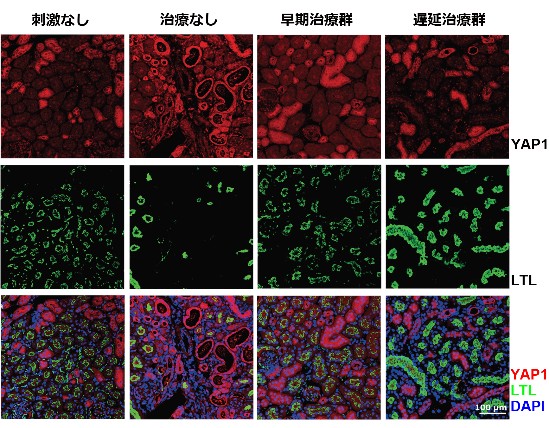
線維化進行によりYAP1の発現が増強し、核内にもシグナルが検出される(治療なし)。化合物3kを投与するとYAP1の染色強度は正常レベル程度に低下した(早期および遅延治療群)。これらの治療群では、LTL染色陽性細胞が維持されており、尿細管の萎縮に対しても抑制、改善効果が得られた。(各群は図2-i,iii,iv,vに対応)(Kosakai et al. (2026) JBC, doi:10.1016/j.jbc.2025.111029より改変)
さらに、ヒト腎臓由来のHK2細胞を用いた線維化モデル系においても、線維化促進因子であるCCN2の発現誘導が化合物3kによって抑制されることが確認されました(図4A, B)。細胞を分画してウエスタンブロット解析を行い、化合物3kがPKM2、YAP1、β-カテニン(YAP1と同様に、線維化に関わる遺伝子の転写調節因子)の核内移行を抑制することを明らかにしました(図4C)。また、共免疫沈降実験により、線維化を誘導されたHK2細胞(図4A, Vehicle処理群)ではPKM2がYAP1およびβ-カテニンと複合体を形成することを証明しました。
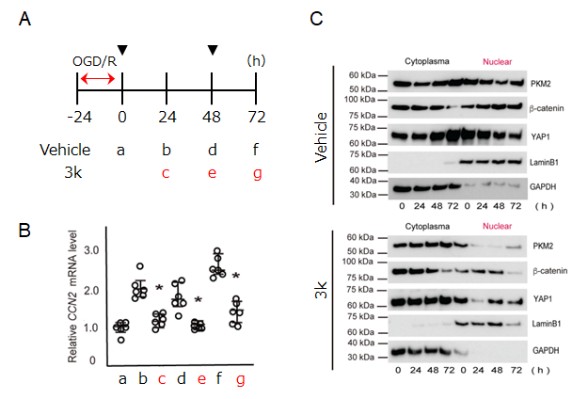
A, ヒト腎臓細胞HK-2に虚血再灌流刺激(OGD/R)による線維化を誘導し、0、48時間後(▼)にDMSO(Vehicle)または化合物3k(3k)を投与した。B, 定量的PCR解析。化合物3kは刺激により誘導される線維化促進遺伝子CCN2の発現増加を抑制した(b, d, f対c, e, g)。C, ウエスタンブロット解析。刺激を受けた細胞では、核内にPKM2、β-カテニン、YAP1が検出される(Vehicle(上図), Nuclear)。化合物3k存在下では、いずれの分子についても核内移行が減少した(3k(下図), Nuclear)。(Kosakai et al. (2026) JBC, doi:10.1016/j.jbc.2025.111029より改変)
■今後の展望■
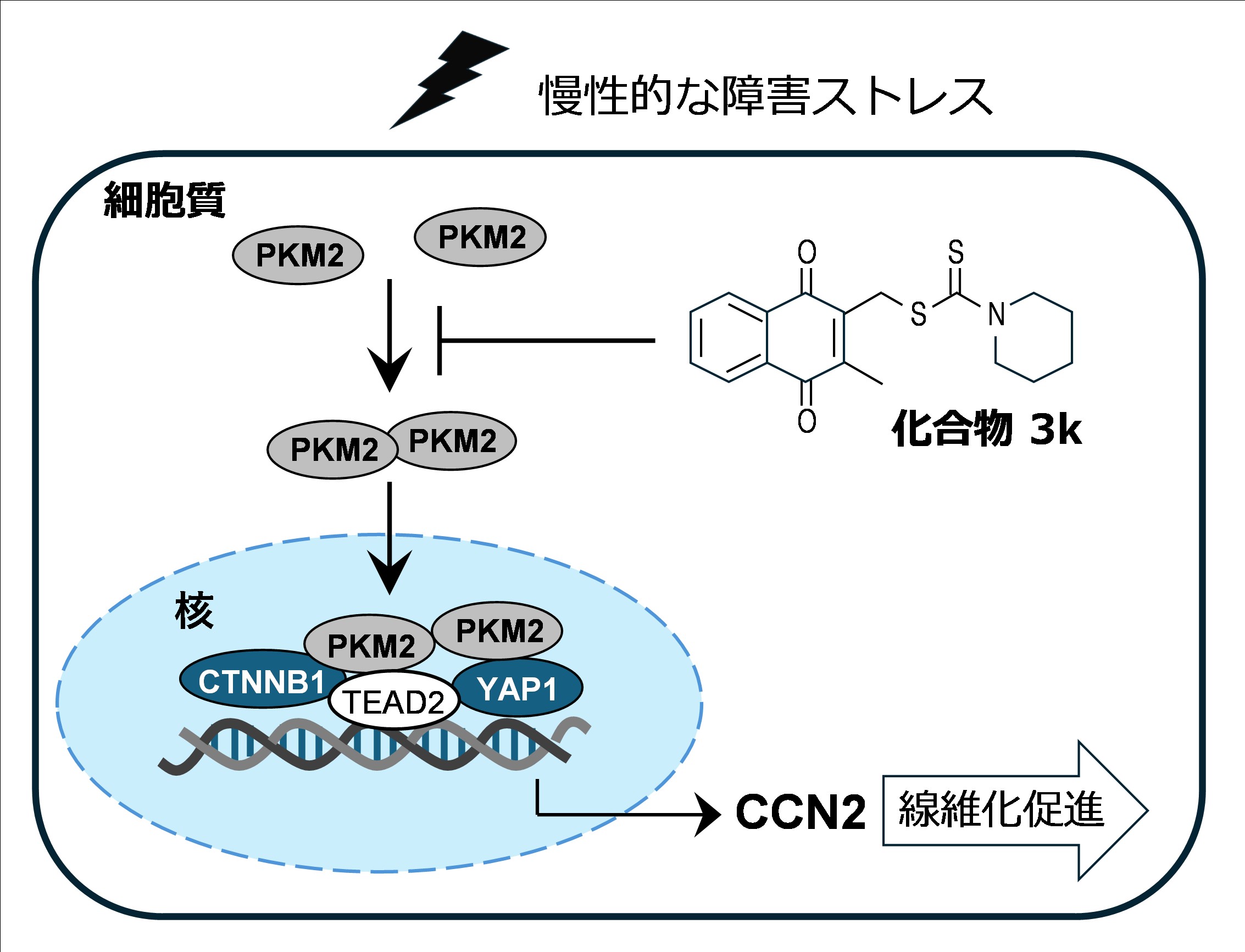
本研究により、PKM2が線維化を引き起こす遺伝子のスイッチを入れる「転写補助因子」として働くことが明らかになりました(図5)。
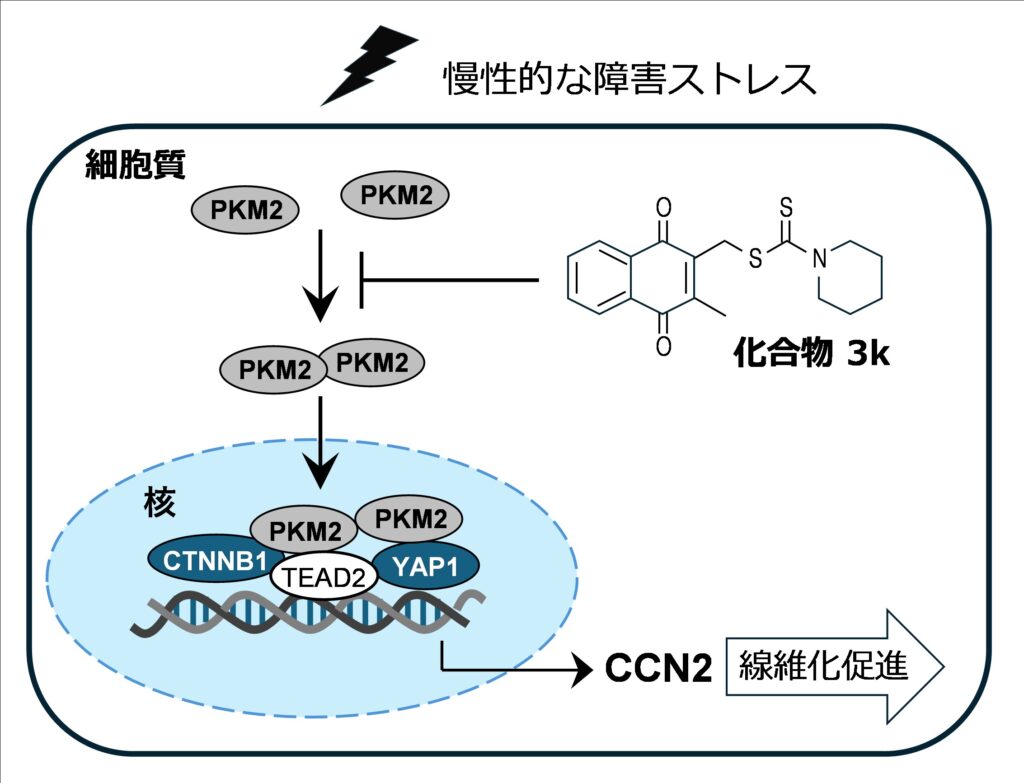
(Kosakai et al. (2026) JBC, doi:10.1016/j.jbc.2025.111029より改変)
慢性的な障害ストレスの存在下で、PKM2は細胞質から核内へと移行、YAP1やβ-カテニンと複合体を形成します。化合物3kはPKM2の核移行過程を抑制する阻害活性を持ち、この作用は腎障害が進行してから投与しても障害の回復に有効でした。化合物3kはヒト慢性腎臓病の新規治療薬を開発する上で重要な出発点となる化合物です。
今後は、患者さんが服用できる経口薬とするため、溶解性やバイオアベイラビリティ、特異性の改善を進めるとともに、臨床研究で有効性の検証を行い、早期の実用化を目指します。
■研究資金■
本研究は、文部科学省科学研究費補助金の助成を受けて実施されました。ご支援に感謝申し上げます。
■論文の情報■
論文名:PKM2 inhibitor suppresses kidney fibrogenesis by disrupting YAP-TEAD-CCN2 transcriptional signaling following ischemia–reperfusion injury
雑誌名:Journal of Biological Chemistry
著 者:Wakako Kosakai, Tsutomu Inoue, Tetsuya Sato, and Hirokazu Okada
U R L:https://doi.org/10.1016/j.jbc.2025.111029
■用語の説明■
*1) PKM2(ピルビン酸キナーゼM2):解糖系の最終段階を触媒する酵素。腎障害時には核内に移行し、線維化を促進する遺伝子のスイッチを入れる転写補助因子として働く。
*2) CCN2(結合組織成長因子/CTGF):線維化を促進するタンパク質。コラーゲン産生や筋線維芽細胞への分化を誘導する。
*3) 化合物3k:PKM2の選択的阻害剤(CAS No. 94164-88-2)。PKM2の酵素活性および核内移行を阻害し、線維化を抑制する。
*4) YAP1:Hippoシグナル経路の下流エフェクター。核内でTEADファミリーと結合し、細胞増殖や線維化関連遺伝子の発現を促進する。
*5) β-カテニン:細胞接着や遺伝子発現の調節に関わるタンパク質。核内に移行すると線維化を促進する遺伝子の発現を誘導する。
*6) RAA系阻害薬(レニン・アンジオテンシン・アルドステロン系阻害薬):血圧を上げるホルモンの働きを抑える薬。ACE阻害薬やARBなどがあり、血圧を下げるとともに腎臓を保護する効果がある。
*7) SGLT2阻害薬:尿から糖を排出させることで血糖値を下げる糖尿病治療薬。近年、糖尿病の有無にかかわらず腎臓を保護する効果があることがわかり、慢性腎臓病の治療薬としても使用されている。
※取材の際には、事前に下記までご一報くださいますようお願い申し上げます。
⊳ 研究についてのお問い合わせ
岡田 浩一(おかだ ひろかず)
埼玉医科大学 医学部 腎臓内科 教授・部長
TEL: 049-276-1611
Email: okada.hirokazu@1972.saitama-med.ac.jp
⊳ 取材、報道についてのお問い合わせ
学校法人 埼玉医科大学
広報室(担当:蒔田)
TEL: 049-276-2125
Email: koho@saitama-med.ac.jp