【中部大学】ウイルスを使わずマウス体内で「巨大な染色体再編成」の誘導・修復に成功ー疾患モデル作製とDNA修復研究の新たな基盤へー
1.研究成果のポイント
- ウイルスを使わない「非ウイルス性」の手法で、マウス生体内の染色体操作に成功
- 57.8 Mb(1Mbは100万塩基対)に及ぶ超長距離の逆位修復を実証
- がん関連の「融合遺伝子」を含む、多様で複雑な構造変異を誘導
2.発表概要
染色体の配列が入れ替わる「染色体再編成」は、がんや先天性疾患の主要な原因となります。これまで、生体内の体細胞でこのような大規模な変異を操作する試みは主にウイルスベクター (注1) を用いて行われてきましたが、ウイルスの使用には、搭載できる遺伝子サイズの制限や、酵素の持続発現による意図しない部位の切断(オフターゲット効果)といった課題がありました。
中部大学大学院 生命健康科学研究科 生命医科学専攻の岩田悟講師、岩本隆司教授らは、マウス子宮内腔へCRISPR/Cas9タンパク質とガイドRNAの複合体(RNP)(注2) を注入し、電気パルス(エレクトロポレーション)によって導入する手法を応用しました。この一過性の「非ウイルス性」手法により、子宮上皮細胞において狙い通りの染色体再編成を引き起こすことに成功しました (図1)。
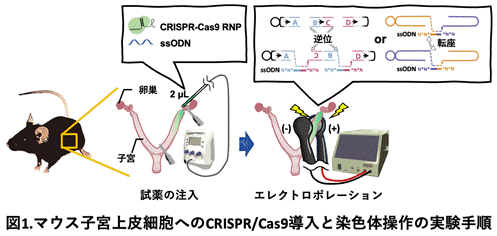
本研究では、57.8 Mbという超長距離を隔てた染色体切断端が、一塩基レベルの精度で修復されることを確認しました。また、本手法を用いて子宮肉腫の原因とされる「融合遺伝子」の誘導にも成功しており、本手法の適用範囲の広さを示しています。
本手法はあくまでも基礎研究のための実験ツールであり、現時点では疾患の治療への応用を意図したものではありません。また、各染色体再編成イベントの検出頻度は限られており、手法のさらなる改良が今後の課題です。しかし、特定の疾患に関連する染色体再編成を持つマウスを迅速に作製するツールとして、また、体細胞における染色体の修復メカニズムを理解するための新たな研究基盤として貢献することが期待されます。
研究成果の詳細は、5月11日付(米国太平洋標準時)で、国際的な医学と科学の専門誌PLOS ONEに掲載されました。本研究はJSPS科研費(23K21287、25K23678)、日本私立学校振興・共済事業団 学術研究振興資金、および中部大学グラント(S)による助成を受けて行われました。
3.論文情報
雑誌名:PLOS ONE
論文タイトル:Non-viral in vivo electroporation-based chromosomal engineering and repair assessment in the murine uterine epithelium
著者:Satoru Iwata, Yumi Miura, Takashi Iwamoto
DOI:10.1371/journal.pone.0348797
4.用語解説
注1:ウイルスベクター
遺伝子を細胞内に運ぶために、ウイルスの感染能力を利用して「運び屋」としたもの。ゲノム編集などで広く使われますが、種類によってDNAサイズの制限、免疫反応の誘発、染色体への組み込みによるリスクなど、それぞれ異なる課題があります。
注2:CRISPR/Cas9 RNP
DNAを切断する酵素(Cas9)と標的を指定するRNA(gRNA)の複合体。細胞内ですぐに作用し短期間で分解されるため、ウイルスを使う手法よりも「その時だけ」作用させることができ、安全性が高いのが特徴です。
5.お問い合わせ先
(研究内容について)
中部大学大学院 生命健康科学研究科 生命医科学専攻 岩田悟講師
Eメール:satoru_iwata@fsc.chubu.ac.jp
本件に関するお問い合わせ先
中部大学 入試・広報センター(広報課)
- TEL
- 0568-51-5541
- chubu-info@fsc.chubu.ac.jp