- ★Google+
- ★Hatena::Bookmark
【 ポイント 】
機能未知リソソーム膜タンパク質SLC46A3が、リソソーム内の有機アニオン化合物や抗体-薬物複合体(ADC)から産生される薬物を細胞質内へ排出することを世界で初めて同定しました。さらに本発見により、現在、乳がん治療薬として用いられるADC、トラスツズマブ エムタンシンの作用機序の一端が明らかになりました。本知見は、新規ADC開発やエンドサイトーシスを介した様々な創薬モダリティの薬物送達への応用に役立つことが期待されます。
【 概 要 】
近年、抗体-薬物複合体(Antibody Drug Conjugate: ADC)(注1)や中分子医薬品(分子量:500-5,000)が創薬モダリティ(注2)として注目を浴びています。これら医薬品は、従来型の低分子医薬品とは異なり、生体膜透過性が低いため、抗体や特殊なキャリアーを利用して標的細胞へ送達させ、エンドサイトーシス(注3)機構により細胞内へ取り込ませる必要があります。取り込まれた医薬品は、細胞内で処理され、最終的にリソソーム(注4)に到達しますが、やはりここにも生体膜(リソソーム膜)が存在し、遊離した薬物や中分子医薬品がその膜を容易に通過できないため、これら医薬品が十分な薬効を発揮するためにはリソソームから薬物を効率的に取り出すことが重要となります。しかし、これまでリソソームでの「医薬品の出口」に関する知見はほとんどありませんでした。
今回、東京薬科大学 薬学部 薬物動態制御学教室の井上勝央教授、東京大学 医学部の高田龍平講師(東京大学医学部附属病院 薬剤部長)らの研究グループは、機能不明であったリソソーム膜タンパク質SLC46A3がリソソーム内のステロイド抱合体や胆汁酸などの有機アニオン化合物を細胞質内へ輸送するトランスポーター(注5)であることを世界で初めて明らかにしました(図1)。SLC46A3は、有機アニオン化合物に限らず、現在、乳がん治療に使用されるADCであるトラスツズマブ エムタンシン(T-DM1)の活性代謝物(Lys-SMCC-DM1、分子量:1,103.7、図1下)に対する輸送活性も有することが示されました(図2)。さらに、SLC46A3の機能を阻害する医薬品を同定し、それら医薬品との共存下において、乳がん細胞株に対するT-DM1の殺細胞効果が減弱することも見出しました(図3)。
本研究成果は、リソソーム内から多様な化合物を取り出すための分子機構の存在を明らかにするとともに、その取り出しの可否にSLC46A3による認識性が関与する可能性を示しています。今後、SLC46A3により認識される化合物の構造を解析することにより、容易にリソソームから脱出できる医薬品の開発が可能となり、より有効な新規創薬モダリティの開発に役立つと期待されます。
本研究は、日本学術振興会 科学研究費助成事業などの支援により実施されたものであり、5月20日(イギリス現地時間)、学術誌「PNAS Nexus」オンライン版で公開されました。
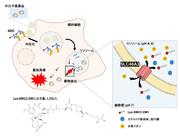
図1 リソソーム輸送体を利用した薬物送達の概念図と今回明らかとなったSLC46A3の分子機能
エンドサイトーシスにより内在化されたADCや中分子医薬品は、リソソームに到達し、リソソーム内で薬物本体を遊離する。遊離した薬物がリソソームから細胞質に移行することで薬効を発揮するが、そのリソソーム膜を介した薬物移行に関する詳細は不明であった。本研究により、リソソーム膜タンパク質SLC46A3がプロトン(水素イオン)濃度勾配を利用して、ステロイド抱合体や胆汁酸などの有機アニオン化合物やトラスツズマブ エムタンシン(T-DM1)の活性代謝物(Lys-SMCC-DM1)をリソソーム内から細胞質へ輸送することが明らかになった。
図2 SLC46A3によるLys-SMCC-DM1輸送活性
通常リソソームに局在するSLC46A3を細胞膜に局在するように改変し(SLC46A3 dC)、Lys-SMCC-DM1の細胞内取り込みを評価した。その結果、対照細胞と比較して、SLC46A3 dC発現細胞ではLys-SMCC-DM1が顕著に細胞内に取り込まれることが明らかとなった(左)。また、細胞外pH 7.4では輸送活性を示さない一方、細胞外pH 5.0で顕著な輸送活性を示すことが明らかとなった(右)。
図3 SLC46A3輸送活性と乳がん細胞に対するT-DM1の殺細胞効果に対する各種医薬品の影響
SLC46A3 dC介在性Lys-SMCC-DM1輸送活性に対する各種医薬品の影響を検討した結果、マクロライド系抗菌薬や抗結核薬のリファブチンにより顕著に阻害されることが明らかとなった(左)。さらに、乳がん細胞を用いて、T-DM1による殺細胞効果に対するSLC46A3阻害剤(クラリスロマイシン)の影響を検討した結果、クラリスロマイシン存在下においてT-DM1作用時の細胞生存率が顕著に上昇したことから、SLC46A3阻害剤はT-DM1の殺細胞効果を減弱することが明らかとなった(右)。
発表雑誌
雑誌名:PNAS Nexus
論文名:SLC46A3 is a lysosomal proton-coupled steroid conjugate and bile acid transporter involved in transport of active catabolites of T-DM1
著者:Ryuto Tomabechi (苫米地 隆人、筆頭著者)1, Hisanao Kishimoto1, Taeka Sato1, Naoki Saito1, Keisuke Kiyomiya1, Tappei Takada2, Kei Higuchi1, Yoshiyuki Shirasaka3, and Katsuhisa Inoue (井上勝央、責任著者)1
1 Department of Biopharmaceutics, School of Pharmacy, Tokyo University of Pharmacy and Life Sciences
2 Department of Pharmacy, The University of Tokyo Hospital
3 Faculty of Pharmacy, Institute of Medical, Pharmaceutical and Health Sciences, Kanazawa University
Doi: https://doi.org/10.1093/pnasnexus/pgac063
用語解説
(注1)抗体-薬物複合体:抗体に抗がん剤などの薬物を付与したもの。抗体が細胞表面に特定の分子をもつがん細胞に結合する性質を利用して、薬物をがん細胞に届け、そこで薬物を放出することで、抗腫瘍効果を発揮する。
(注2)創薬モダリティ:低分子医薬や抗体医薬、核酸医薬のような様々な分子医薬品の創薬基盤技術の方法・手段の分類を表す用語。
(注3)エンドサイトーシス:細胞が外部の物質を取り込む過程の一つ。細胞の表面で、細胞膜の一部が物質を包み込むようにして陥没し、細胞膜から遊離して小胞を形成する。
(注4)リソソーム:細胞内小器官の一つ。内部には酸性領域に至適pHをもつ様々な加水分解酵素を含み、エンドサイトーシスにより細胞外から取り込んだ高分子化合物を分解する。リソソーム膜には最終分解産物であるアミノ酸、糖、および核酸などの栄養素を細胞質に送り出すトランスポーターが存在し、分解産物の再利用に重要である。リソソームは細胞内の分解装置としてだけでなく、損傷した細胞膜の修復や細胞内の栄養状態(アミノ酸など)を感知する場としても重要である。
(注5)トランスポーター:生体膜に存在し、細胞内外の物質(生体内物質や栄養素、薬物など)の輸送を担う膜タンパク質の総称。
近年、抗体-薬物複合体(Antibody Drug Conjugate: ADC)(注1)や中分子医薬品(分子量:500-5,000)が創薬モダリティ(注2)として注目を浴びています。これら医薬品は、従来型の低分子医薬品とは異なり、生体膜透過性が低いため、抗体や特殊なキャリアーを利用して標的細胞へ送達させ、エンドサイトーシス(注3)機構により細胞内へ取り込ませる必要があります。取り込まれた医薬品は、細胞内で処理され、最終的にリソソーム(注4)に到達しますが、やはりここにも生体膜(リソソーム膜)が存在し、遊離した薬物や中分子医薬品がその膜を容易に通過できないため、これら医薬品が十分な薬効を発揮するためにはリソソームから薬物を効率的に取り出すことが重要となります。しかし、これまでリソソームでの「医薬品の出口」に関する知見はほとんどありませんでした。
今回、東京薬科大学 薬学部 薬物動態制御学教室の井上勝央教授、東京大学 医学部の高田龍平講師(東京大学医学部附属病院 薬剤部長)らの研究グループは、機能不明であったリソソーム膜タンパク質SLC46A3がリソソーム内のステロイド抱合体や胆汁酸などの有機アニオン化合物を細胞質内へ輸送するトランスポーター(注5)であることを世界で初めて明らかにしました(図1)。SLC46A3は、有機アニオン化合物に限らず、現在、乳がん治療に使用されるADCであるトラスツズマブ エムタンシン(T-DM1)の活性代謝物(Lys-SMCC-DM1、分子量:1,103.7、図1下)に対する輸送活性も有することが示されました(図2)。さらに、SLC46A3の機能を阻害する医薬品を同定し、それら医薬品との共存下において、乳がん細胞株に対するT-DM1の殺細胞効果が減弱することも見出しました(図3)。
本研究成果は、リソソーム内から多様な化合物を取り出すための分子機構の存在を明らかにするとともに、その取り出しの可否にSLC46A3による認識性が関与する可能性を示しています。今後、SLC46A3により認識される化合物の構造を解析することにより、容易にリソソームから脱出できる医薬品の開発が可能となり、より有効な新規創薬モダリティの開発に役立つと期待されます。
本研究は、日本学術振興会 科学研究費助成事業などの支援により実施されたものであり、5月20日(イギリス現地時間)、学術誌「PNAS Nexus」オンライン版で公開されました。
図1 リソソーム輸送体を利用した薬物送達の概念図と今回明らかとなったSLC46A3の分子機能
エンドサイトーシスにより内在化されたADCや中分子医薬品は、リソソームに到達し、リソソーム内で薬物本体を遊離する。遊離した薬物がリソソームから細胞質に移行することで薬効を発揮するが、そのリソソーム膜を介した薬物移行に関する詳細は不明であった。本研究により、リソソーム膜タンパク質SLC46A3がプロトン(水素イオン)濃度勾配を利用して、ステロイド抱合体や胆汁酸などの有機アニオン化合物やトラスツズマブ エムタンシン(T-DM1)の活性代謝物(Lys-SMCC-DM1)をリソソーム内から細胞質へ輸送することが明らかになった。
図2 SLC46A3によるLys-SMCC-DM1輸送活性
通常リソソームに局在するSLC46A3を細胞膜に局在するように改変し(SLC46A3 dC)、Lys-SMCC-DM1の細胞内取り込みを評価した。その結果、対照細胞と比較して、SLC46A3 dC発現細胞ではLys-SMCC-DM1が顕著に細胞内に取り込まれることが明らかとなった(左)。また、細胞外pH 7.4では輸送活性を示さない一方、細胞外pH 5.0で顕著な輸送活性を示すことが明らかとなった(右)。
図3 SLC46A3輸送活性と乳がん細胞に対するT-DM1の殺細胞効果に対する各種医薬品の影響
SLC46A3 dC介在性Lys-SMCC-DM1輸送活性に対する各種医薬品の影響を検討した結果、マクロライド系抗菌薬や抗結核薬のリファブチンにより顕著に阻害されることが明らかとなった(左)。さらに、乳がん細胞を用いて、T-DM1による殺細胞効果に対するSLC46A3阻害剤(クラリスロマイシン)の影響を検討した結果、クラリスロマイシン存在下においてT-DM1作用時の細胞生存率が顕著に上昇したことから、SLC46A3阻害剤はT-DM1の殺細胞効果を減弱することが明らかとなった(右)。
発表雑誌
雑誌名:PNAS Nexus
論文名:SLC46A3 is a lysosomal proton-coupled steroid conjugate and bile acid transporter involved in transport of active catabolites of T-DM1
著者:Ryuto Tomabechi (苫米地 隆人、筆頭著者)1, Hisanao Kishimoto1, Taeka Sato1, Naoki Saito1, Keisuke Kiyomiya1, Tappei Takada2, Kei Higuchi1, Yoshiyuki Shirasaka3, and Katsuhisa Inoue (井上勝央、責任著者)1
1 Department of Biopharmaceutics, School of Pharmacy, Tokyo University of Pharmacy and Life Sciences
2 Department of Pharmacy, The University of Tokyo Hospital
3 Faculty of Pharmacy, Institute of Medical, Pharmaceutical and Health Sciences, Kanazawa University
Doi: https://doi.org/10.1093/pnasnexus/pgac063
用語解説
(注1)抗体-薬物複合体:抗体に抗がん剤などの薬物を付与したもの。抗体が細胞表面に特定の分子をもつがん細胞に結合する性質を利用して、薬物をがん細胞に届け、そこで薬物を放出することで、抗腫瘍効果を発揮する。
(注2)創薬モダリティ:低分子医薬や抗体医薬、核酸医薬のような様々な分子医薬品の創薬基盤技術の方法・手段の分類を表す用語。
(注3)エンドサイトーシス:細胞が外部の物質を取り込む過程の一つ。細胞の表面で、細胞膜の一部が物質を包み込むようにして陥没し、細胞膜から遊離して小胞を形成する。
(注4)リソソーム:細胞内小器官の一つ。内部には酸性領域に至適pHをもつ様々な加水分解酵素を含み、エンドサイトーシスにより細胞外から取り込んだ高分子化合物を分解する。リソソーム膜には最終分解産物であるアミノ酸、糖、および核酸などの栄養素を細胞質に送り出すトランスポーターが存在し、分解産物の再利用に重要である。リソソームは細胞内の分解装置としてだけでなく、損傷した細胞膜の修復や細胞内の栄養状態(アミノ酸など)を感知する場としても重要である。
(注5)トランスポーター:生体膜に存在し、細胞内外の物質(生体内物質や栄養素、薬物など)の輸送を担う膜タンパク質の総称。
【取材に関するお問い合わせ先】
東京薬科大学 総務部広報課
TEL:042-676-6711 mail:kouhouka@toyaku.ac.jp
【研究に関するお問い合わせ先】
東京薬科大学 薬学部 薬物動態制御学教室 教授 井上勝央
TEL:042-676-3126 mail:kinoue@toyaku.ac.jp
東京薬科大学 総務部広報課
TEL:042-676-6711 mail:kouhouka@toyaku.ac.jp
【研究に関するお問い合わせ先】
東京薬科大学 薬学部 薬物動態制御学教室 教授 井上勝央
TEL:042-676-3126 mail:kinoue@toyaku.ac.jp
▼本件に関する問い合わせ先 |
|
総務部 広報課 | |
住所 | : 東京都八王子市堀之内1432-1 |
TEL | : 0426766711 |
FAX | : 042-676-1633 |
大学・学校情報 |
|---|
| 大学・学校名 東京薬科大学 |

|
| URL https://www.toyaku.ac.jp/ |
| 住所 東京都八王子市堀之内1432-1 |
| 学長(学校長) 三巻 祥浩 |


 大学探しナビで東京薬科大学の情報を見る
大学探しナビで東京薬科大学の情報を見る