脳腫瘍でmTORを活性化する新たな仕組みの解明 ~脳腫瘍の新たな治療法の開発が期待される–北里大学
北里大学理学部生物科学科の堤 弘次講師、野原 歩(北里大学大学院理学研究科修士課程修了)らのグループは、mTORの活性を制御する新たな経路を明らかにし、この経路を阻害することで脳腫瘍の形成を抑制することを発見しました。
mTORは酵母からヒトまで全ての真核生物で代謝を制御する鍵となる酵素です。mTORは脳腫瘍をはじめとした様々ながんで、酵素活性が上昇することによって、腫瘍の形成に関わっており、抗がん剤の標的としても注目されています。しかしmTORが脳腫瘍でなぜ活性化しているかは不明でした。今回、FilGAPタンパク質が脳腫瘍細胞でmTORを活性化していることを発見し、FilGAPの発現阻害により脳腫瘍形成モデルであるスフェロイドの成長を抑制することに成功しました。本研究成果は、新たな脳腫瘍の治療法の開発や、脳腫瘍の悪性化マーカーの開発へと繋がることが期待されます。
本研究成果は、2023年12月8日(金)19時(日本時間)に、英国電子科学雑誌「Scientific Reports」にオンライン掲載されました。
本研究成果は、2023年12月8日(金)19時(日本時間)に、英国電子科学雑誌「Scientific Reports」にオンライン掲載されました。
■研究成果のポイント
・抗がん剤の標的としても注目されるmTORの新たな活性化の仕組みを明らかにした。
・FilGAPはmTOR複合体と結合し、活性を促進することを発見した。
・脳腫瘍ではFilGAPの特定の転写アイソフォームの発現が増加していた。
・脳腫瘍細胞でFilGAPの発現を阻害することで、腫瘍形成モデルであるスフェロイド形成を抑制することに成功した。
・本研究の成果は新たな脳腫瘍の治療戦略の開発へと繋がることが期待される。
・抗がん剤の標的としても注目されるmTORの新たな活性化の仕組みを明らかにした。
・FilGAPはmTOR複合体と結合し、活性を促進することを発見した。
・脳腫瘍ではFilGAPの特定の転写アイソフォームの発現が増加していた。
・脳腫瘍細胞でFilGAPの発現を阻害することで、腫瘍形成モデルであるスフェロイド形成を抑制することに成功した。
・本研究の成果は新たな脳腫瘍の治療戦略の開発へと繋がることが期待される。
■背景
グリオーマは悪性の脳腫瘍であり、その悪性度によってグレードII〜VIに分類されます。最も悪性度の高いグレードVIの膠芽腫は5年生存率が10%以下と非常に予後が悪く、その治療法や早期診断法の開発は、健康維持と生活の質を向上させるために非常に重要です。
mTORは酵母からヒトまで保存された、生物の成長、増殖、老化を制御する重要なタンパク質リン酸化酵素です。mTORは細胞内で多くのタンパク質が集合した複合体を形成することで働くことができます。この複合体を構成するタンパク質の種類によってmTORは、mTORC1とmTORC2という異なる働きを持つ複合体を形成します。mTORの酵素活性が上昇することで、身体の様々な部位に腫瘍が形成されることが分かっています。しかし、がんでmTORが活性化する仕組みは不明な点が多く残されています。
グリオーマは悪性の脳腫瘍であり、その悪性度によってグレードII〜VIに分類されます。最も悪性度の高いグレードVIの膠芽腫は5年生存率が10%以下と非常に予後が悪く、その治療法や早期診断法の開発は、健康維持と生活の質を向上させるために非常に重要です。
mTORは酵母からヒトまで保存された、生物の成長、増殖、老化を制御する重要なタンパク質リン酸化酵素です。mTORは細胞内で多くのタンパク質が集合した複合体を形成することで働くことができます。この複合体を構成するタンパク質の種類によってmTORは、mTORC1とmTORC2という異なる働きを持つ複合体を形成します。mTORの酵素活性が上昇することで、身体の様々な部位に腫瘍が形成されることが分かっています。しかし、がんでmTORが活性化する仕組みは不明な点が多く残されています。
■研究内容と成果
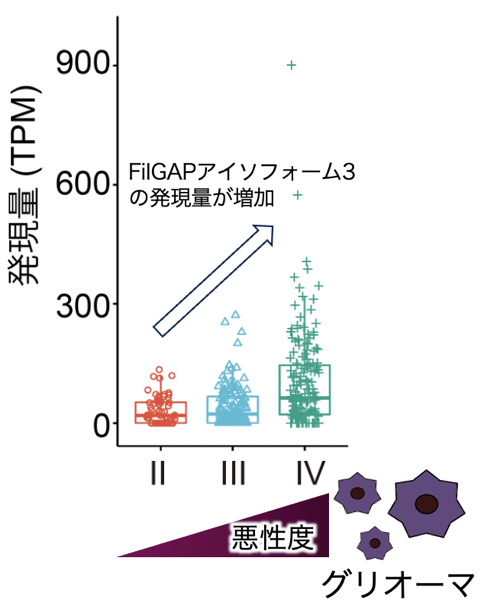
今回研究グループは、ARHGAP24遺伝子産物であるFilGAPが、グリオーマ細胞でmTOR複合体と相互作用することを発見しました。また、FilGAPはグリオーマ細胞でmTORC1及びmTORC2の酵素活性を上昇させることを明らかにしました。グリオーマ細胞ではサイズが小さなFilGAPの転写アイソフォーム(アイソフォーム3)が高発現しており、この転写アイソフォームが最も悪性度の高い膠芽腫の患者脳で高発現していることが分かりました【図1】。また、FilGAPによるmTORC2の活性化は、mTORを活性化する経路であるPI3K経路非依存的であることが示唆されました。そしてグリオーマ細胞でFilGAPの発現を阻害することで、腫瘍形成モデルであるスフェロイドの成長を抑えることに成功しました【図2】。
今回研究グループは、ARHGAP24遺伝子産物であるFilGAPが、グリオーマ細胞でmTOR複合体と相互作用することを発見しました。また、FilGAPはグリオーマ細胞でmTORC1及びmTORC2の酵素活性を上昇させることを明らかにしました。グリオーマ細胞ではサイズが小さなFilGAPの転写アイソフォーム(アイソフォーム3)が高発現しており、この転写アイソフォームが最も悪性度の高い膠芽腫の患者脳で高発現していることが分かりました【図1】。また、FilGAPによるmTORC2の活性化は、mTORを活性化する経路であるPI3K経路非依存的であることが示唆されました。そしてグリオーマ細胞でFilGAPの発現を阻害することで、腫瘍形成モデルであるスフェロイドの成長を抑えることに成功しました【図2】。
■今後の展開
本研究によって、FilGAPがmTORに結合し活性化することを世界で初めて明らかにし、そしてFilGAPの発現を阻害することで脳腫瘍の成長を抑えられることを発見しました【図3】。また、膠芽腫でFilGAPの特定の短い転写アイソフォームの発現量が増加していたことから、この発現量の増加がグリオーマの悪性化に関わっている可能性が考えられます。グリオーマにおけるFilGAPの転写アイソフォームの発現の仕組みとその悪性化との関係を解析することで、グリオーマの悪性化の仕組みの解明に繋がることが期待されます。さらにFilGAPによるmTORの活性化はPI3K経路非依存的であることも示唆されました。この結果はFilGAPが薬物耐性を持つがん細胞の増殖に関わることも示唆しております。そのため、今回の成果からFilGAPを標的とした新たな創薬や、脳腫瘍の治療戦略の開発へと発展することも大きく期待されます。
本研究によって、FilGAPがmTORに結合し活性化することを世界で初めて明らかにし、そしてFilGAPの発現を阻害することで脳腫瘍の成長を抑えられることを発見しました【図3】。また、膠芽腫でFilGAPの特定の短い転写アイソフォームの発現量が増加していたことから、この発現量の増加がグリオーマの悪性化に関わっている可能性が考えられます。グリオーマにおけるFilGAPの転写アイソフォームの発現の仕組みとその悪性化との関係を解析することで、グリオーマの悪性化の仕組みの解明に繋がることが期待されます。さらにFilGAPによるmTORの活性化はPI3K経路非依存的であることも示唆されました。この結果はFilGAPが薬物耐性を持つがん細胞の増殖に関わることも示唆しております。そのため、今回の成果からFilGAPを標的とした新たな創薬や、脳腫瘍の治療戦略の開発へと発展することも大きく期待されます。
■論文情報
・掲載雑誌名:Scientific Reports
・論文名:FilGAP regulates tumor growth in Glioma through the regulation of mTORC1 and mTORC2
・著者名:堤 弘次(筆頭著者、責任著者)、野原 歩(筆頭著者)、田中 大稀、村野 萌、宮垣 柚里奈、太田 安隆(責任著者)
・DOI:10.1038/s41598-023-47892-1
・掲載雑誌名:Scientific Reports
・論文名:FilGAP regulates tumor growth in Glioma through the regulation of mTORC1 and mTORC2
・著者名:堤 弘次(筆頭著者、責任著者)、野原 歩(筆頭著者)、田中 大稀、村野 萌、宮垣 柚里奈、太田 安隆(責任著者)
・DOI:10.1038/s41598-023-47892-1
※本研究は北里大学学術奨励研究の助成を受けたものです。
■用語説明
・FilGAP:低分子量Gタンパク質Racの活性を制御することで細胞の運動、接着を制御するタンパク質として知られる当研究室で単離されたタンパク質。
・転写アイソフォーム:同じ遺伝子から転写開始点や開始コドンの違いから生まれる異なる転写産物。転写バリアントとも呼ばれる。
・スフェロイド:細胞同士が凝集して形成される球状の細胞塊。生体内で形成される腫瘍と似た性質を持っている。
・タンパク質リン酸化酵素:標的タンパク質にリン酸を付加する、リン酸化反応を行う酵素。標的タンパク質がリン酸化されることで、タンパク質の構造や活性が変化する。
・PI3K:ホスファチジルイノシトール3-キナーゼは細胞膜の構成成分であるPIP3(ホスファチジルイノシトール3リン酸)を作る。多くのがん細胞ではPIP3が増加し、これが異常な増殖を引き起こす。
・TCGA:The Cancer Genome Atlasは米国の研究所が実施するプロジェクトで、がん関連の遺伝子発現異常についての包括的データベースを提供する。
・FilGAP:低分子量Gタンパク質Racの活性を制御することで細胞の運動、接着を制御するタンパク質として知られる当研究室で単離されたタンパク質。
・転写アイソフォーム:同じ遺伝子から転写開始点や開始コドンの違いから生まれる異なる転写産物。転写バリアントとも呼ばれる。
・スフェロイド:細胞同士が凝集して形成される球状の細胞塊。生体内で形成される腫瘍と似た性質を持っている。
・タンパク質リン酸化酵素:標的タンパク質にリン酸を付加する、リン酸化反応を行う酵素。標的タンパク質がリン酸化されることで、タンパク質の構造や活性が変化する。
・PI3K:ホスファチジルイノシトール3-キナーゼは細胞膜の構成成分であるPIP3(ホスファチジルイノシトール3リン酸)を作る。多くのがん細胞ではPIP3が増加し、これが異常な増殖を引き起こす。
・TCGA:The Cancer Genome Atlasは米国の研究所が実施するプロジェクトで、がん関連の遺伝子発現異常についての包括的データベースを提供する。
■問い合わせ先
【研究に関すること】
北里大学理学部生物科学科
講師 堤 弘次
E-mail:k.tutumi@kitasato-u.ac.jp
北里大学理学部生物科学科
講師 堤 弘次
E-mail:k.tutumi@kitasato-u.ac.jp
【報道に関すること】
学校法人北里研究所 総務部広報課
TEL:03-5791-6422
E-mail:kohoh@kitasato-u.ac.jp
学校法人北里研究所 総務部広報課
TEL:03-5791-6422
E-mail:kohoh@kitasato-u.ac.jp