糖脂質(GM3)を標的にしたタンパク尿の新たな治療戦略~透析患者数の減少を目指して~ 北里大学
◆タンパク尿の量が多い腎臓病の患者は透析療法が必要となる危険性が極めて高いが、タンパク尿のみに特化した治療薬は存在しません。
◆抗てんかん薬として知られるバルプロ酸によりGM3合成酵素遺伝子の発現上昇、およびGM3の発現を増強させると、足細胞が保護され、タンパク尿の発症を劇的に予防し、腎臓病(糸球体疾患)の進行が抑制されることを見出しました。このバルプロ酸による予防効果は、GM3合成酵素遺伝子欠損マウスでは全く見られないことから、糖脂質GM3が足細胞の機能維持に重要な役割を果たしていることを明らかにしました。
◆ネフリン障害モデル細胞を用いてGM3が細胞膜においてスリット膜(注2)の構成分子であるネフリンと協調して働いていることを見出したことから、足細胞のGM3発現レベルの亢進は、足細胞の細胞膜環境の改善や障害からの回避効果が高まった結果、タンパク尿が予防されるという機序を明らかにしました。
◆本研究結果は、糖脂質GM3や既存薬の新たな作用を明らかとしたことから、タンパク尿に対する新規治療薬の開発だけでなく、安全面や費用対効果に優れた既存薬であるバルプロ酸を「新しい薬」として活用することで、透析患者数減少への貢献が期待できます。
■研究の背景
慢性腎臓病(注3)は成人の8人中1人に存在していると推定されており、新たな国民病ともいわれています。慢性腎臓病の患者の中でも、タンパク尿の量が多いほど、透析療法や腎移植といった治療が必要となる危険性が高くなることが知られています。腎臓は生物が生きていく過程で生じた老廃物を体外に捨てる仕事をしています。その際、身体に必要なタンパク質が体外に漏れ出ないように、タンパクろ過バリアと呼ばれる「ふるい」の役割をしている場所があります。この「ふるい」が、腎足細胞が形作っているスリット膜と呼ばれる構造物です。タンパク尿はこのろ過バリアが破綻したことで、血液中のタンパク質が尿中に漏れ出てしまう状態で、タンパク尿自体が腎臓病を更に悪化させることが明らかになっています。さらに、タンパク尿がある人は、脳卒中や心筋梗塞などの発症率が約3倍以上になることもわかっています。
これまでも本研究グループは、細胞膜上にある様々な糖タンパク質と糖脂質が互いに協調しながら細胞の機能を維持することを明らかにしてきました。その上で、タンパク尿がでる一部の患者では、主要な糖脂質であるGM3の量が低いほど、タンパク尿が多くなっていることを見出しています(Clin Exp Nephrol. 2022, doi: 10.1007/s10157-022-02249-2)。しかし、GM3がタンパク尿を抑える役割があるか否かは分かっていませんでした。
■研究内容と成果
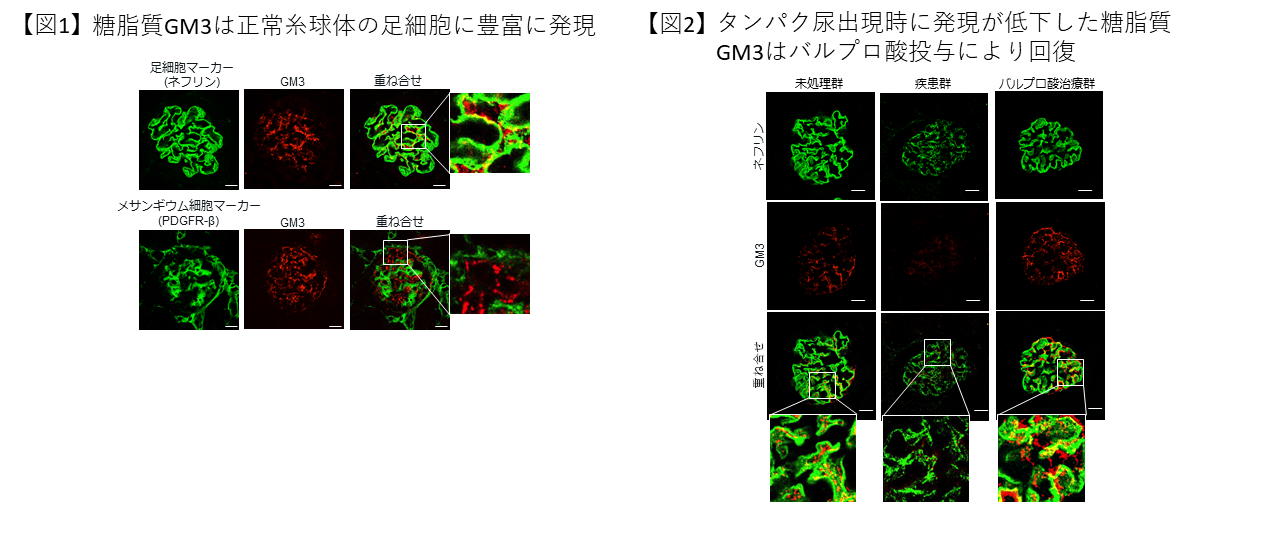
本研究グループは、腎足細胞のスリット膜を形作るネフリンというタンパク質に対する抗体で惹起される腎臓病モデルマウスを樹立しています(Nephron Exp. Nephrol. 138: 71-87. 2017)。このマウスの腎臓を解析したところ、正常の腎臓ではタンパクろ過バリアを形作るネフリンと糖脂質GM3は互いに近くに存在する一方【図1】、抗ネフリン抗体でタンパクろ過バリアが破綻し、タンパク尿が生じると、GM3の発現が低下することを見出しました【図2】。
また以前に、GM3は抗てんかん薬として用いられているバルプロ酸によって発現が増強されることを見出していたことから、抗ネフリン抗体を用いた足細胞障害動物・ネフリン障害細胞モデルを用いて、バルプロ酸によるGM3増強作用が足細胞やネフリンを保護し、その結果タンパク尿を劇的に予防できることを明らかにしました【図3】。さらに、GM3合成酵素遺伝子欠損マウスを用いた解析や発現糖脂質の網羅解析を行い、バルプロ酸は糖脂質の中でもGM3の発現を特異的に亢進させることで、足細胞を保護する効果があることを明らかにしました。
■今後の展開
糖脂質GM3の発現増強によるタンパクろ過バリアの安定化は、タンパク尿の新規治療法開発の戦略として非常に重要であると考えられます。しかし、バルプロ酸を(新しい)タンパク尿治療薬として臨床応用するには解決すべき課題が多くあるため、引き続きこれらの課題の解決に取り組んでいきます。
■論文情報
掲載誌:Scientific Reports
論文名:Glycosphingolipid GM3 prevents albuminuria and podocytopathy induced by anti-nephrin antibody.
著 者:Nagako Kawashima*, Shokichi Naito, Hisatoshi Hanamatsu, Masaki Nagane, Yasuo Takeuchi,
DOI:doi.org/10.1038/s41598-022-20265-w
■用語解説
注1)糸球体足細胞:
腎臓の最初の尿生成過程を行う糸球体に存在する3種類の細胞の一つで、糸球体の最外層に存在しています。糸球体足細胞は、糸球体ろ過バリア機能の維持において最も重要な役割をしている細胞です。また、生体内で最も分化した細胞の一つであり増殖能をもたないことから、治療の際には一つでも多くの足細胞を生存させることが重要とされています。
注2)スリット膜:
糸球体足細胞間に存在する特殊な細胞間接着装置。糸球体のタンパクろ過バリア機能の役割を果たしています。多くの腎疾患では、タンパク尿はスリット膜のバリア機能が障害されることで発症すると考えられています。
注3)慢性腎臓病:
腎臓にどれくらい老廃物を尿へ排泄する能力があるかを調べる数値(eGFR)が60未満になった状態、または持続性のタンパク尿が確認された場合に、慢性腎臓病と診断されます。国内の総患者数は1300万人と推定されていて、慢性腎不全(腎機能が低下し、透析療法、腎移植が必要となる状態)の予備軍とされています。
■研究資金
本研究は、(財)鈴木謙三記念医科学応用研究財団(16-061)、(独)日本学術振興会(JSPS)の科学研究費(17K09709, 18K08249, 20K08615)、および物質・デバイス領域共同研究拠点(20201013)の支援を受けて実施しました。
■その他
本プレスリリースの図は、原論文「Glycosphingolipid GM3 prevents albuminuria and podocytopathy induced by anti-nephrin antibody」の図を引用・改変したものを使用しています。
■問い合わせ先
≪研究に関すること≫
北里大学医学部腎臓内科学
助教 川島永子
E-mail: nagacok@kitasato-u.ac.jp
北里大学医学部腎臓内科学
講師 内藤正吉
E-mail: snaito@med.kitasato-u.ac.jp
≪報道に関すること≫
学校法人北里研究所 総務部広報課
〒108-8641 東京都港区白金5-9-1
TEL: 03-5791-6422
E-mail: kohoh@kitasato-u.ac.jp